پاتوژنها، ماکرومولکولهای زیستی یا موجودات زندهای هستند که در باکتریها، گیاهان و جانوران بیماری ایجاد میکنند. پاتوژنها با تولید پروتئینهای جدید عملکرد سلول میزبان را تغییر میدهند یا با برهمکنش با ماده ژنتیکی میزبان در فرایندهای همانندسازی، رونویسی یا ترجمه اختلال ایجاد میکنند. ویروئیدها، ویروزوئیدها، پریونها و ویروسها پاتوژنهای غیرزنده هستند. ویروئید و ویروزوئید عملکرد سلولهای گیاهی، پریونها عملکرد سلولهای جانوری و ویروسها عملکرد پروکاریوت، سلولهای گیاهی و سلولهای جانوری را تغییر میدهند.
نوع ماده ژنتیکی (DNA یا RNA)، مورفولوژی، شیوه بیماریزایی و شیوه همانندسازی ماده ژنتیکی و شیوه تکثیر پاتوژنها در میزبان متفاوت است. رشد و همانندسازی بعضی از این پاتوژنها کاملا به میزبان وابسته است و در بعضی آنزیمهای همراه پاتوژن به همانندسازی کمک میکنند. در بعضی از این پاتوژنها پوششی پروتئینی یا لیپیدی از ماده ژنتیکی محافظت میکند و در بعضی ماده ژنتیکی بدون پوشش است. در این مطلب از مجله فرادرس ویژگیهای ویروئید را همراه تفاوتهای آن با ویروزوئید، پریون و ویروسها توضیح میدهیم.
ویروئید چیست؟
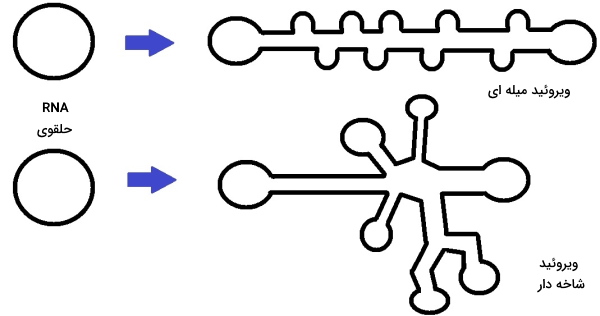
ویروئید یکی از پاتوژنهای سلول گیاهی است که از یک رشته RNA حلقوی و بدون پوشش با ۲۵۰ تا ۴۰۰ ریبونوکلئوتید تشکیل میشود. ویروئیدها از آنزیمها و پروتئینهای سلول میزبان برای تکثیر خود استفاده میکنند. ژن کدکننده پروتئین در این پاتوژنها وجود ندارد. ویروئیدها با عبور از پلاسمودسماتا از سلول آلوده به سلولهای دیگر و بهوسیله آوندهای آبکش به بافتهای دورتر از محل عفونت منتقل میشود. این پاتوژنها از راه پیوند زدن، آسیبهای فیزیکی، گرده، دانه و حشرات بین گیاهان منتقل میشود. این پاتوژنها در گیاهان علفی و چوبی بیماری ایجاد میکنند.
شدت بیماری گیاهان به سویه ویروئید (توالی نوکلئوتیدها)، ژنوتیپ میزبان و شرایط محیطی بستگی دارد. این پاتوژنها با برهمکنش مستقیم با اسیدنوکلئیکهای میزبان بیماری ایجاد میکنند. ویروئیدها بر اساس ساختار دوم به دو خانواده «آوسون ویروئید» (Avsunviroidae) و «پوسپی ویروئید» (Pospiviroidae) تقسیم میشوند. ویژگیهای این دو گروه در جدول زیر مشخص شده است.
| خانواده آوسون ویروئید | خانواده پوسپی ویروئید | |
| ساختار دوم | شبیه Y یا شاخهدار | میلهای |
| دومینهای عملکردی | نامشخص | انتهای چپ (TL)، پاتوژنیک (P)، مرکزی (C)، متنوع (V) و انتهای راست (TR) |
| فعالیت ریبوزیمی | دارد. | ندارد. |
| جایگاه همانندسازی | کلروپلاست میزبان | هسته میزبان |
| روش همانندسازی | چرخش حلقوی متقارن | چرخش حلقوی نامتقارن |
| آنزیمهای همانندسازی | RNA پلیمراز کلروپلاست (وابسته به RNA) | RNA پلیمراز II (وابسته به DNA) |
| میزبان | گیاهان دولپهای علفی و چوبی | گیاهان دولپهای و تکلپهای |
دومین پاتوژنتیک پوسپی ویروئیدها از توالی نوکلئوتیدهای پیریمیدینی (C و T) تشکیل شده و دو رشته RNA در این دومین به راحتی از هم جدا میشود. دومین V تنوع زیادی بین سویههای این ویروئیدها دارد و دومین مرکزی آنها از توالیهای محافظت شده تشکیل میشود. ویروئیدها پس از ورود به سلول میزبان وارد کلروپلاست یا هسته میشوند. از RNA پلیمرازهای میزبان برای تکثیر استفاده میکنند. از سلول پلاسمودسماتا به سلولهای کناری و در نهایت آوند آبکش منتقل میشوند و به تدریج تمام بافتهای گیاه را آلوده میکنند. ویروئید در بیان ژنهای پاسخ به استرسهای محیطی، سیستم دفاعی، فعالیت کلروپلاست و ساختار دیواره سلولی اختلال ایجاد میکنند.
تکثیر ویروئید
ویروئیدها با دو مکانیسم تکحلقهای و دو حلقهای همانندسازی میکنند. در همانندسازی تکحلقهای یا نامتقاون، RNA ویروئید (مثبت یا Sense) پس از چند مرحله رونویسی متوالی به تعداد زیادی RNA خطی منفی (Antisense) تبدیل میشود. این RNAها به هم متصل شده و ساختار چندزیرواحدی ایجاد میکنند. در مرحله بعد از رونویسی RNAهای منفی، RNA مثبت چندزیرواحدی و خطی تشکیل میشود. RNAهای خطی بهوسیله آنزیم RNA پلیمراز II میزبان از هم جدا شده و با کمک RNA لیگاز میزبان، ژنوم حلقوی ویروئید تشکیل میشود.
در همانندسازی دوحلقه یا متقارن، RNA ویروئید (رشته مثبت) پس از چند مرحله رونویسی به تعداد زیادی RNA چند زیرواحدی خطی و منفی تبدیل میشود. این RNAها از هم جدا شده و RNA حلقوی منفی تشکیل میدهند. آنزیمهای میزبان از این RNA به عنوان الگوی ژنوم ویروئید استفاده میکنند. از رونویسی RNA حلقوی منفی تعداد زیادی RNA خطی و چندزیرواحدی مثبت تشکیل میشود. RNA آوسون ویروئیدها فعالیت ریبوزیمی دارد و RNA چند زیرواحدی را به مونومر تبدیل میکند.
تفاوت ویروئید و ویروزوئید چیست؟
ویروزوئیدها گروه دیگری از پاتوژنهای گیاهی هستند. این پاتوژنها از RNA تکرشتهای و حلقوی تشکیل شده است. ویروزوئیدها برای آلوده کردن سلول میزبان و تکثیر به کمک ویروس نیاز دارند. این پاتوژنها در پوشش کپسیدی ویروس وارد سلولهای گیاهی میشوند. این پروتئینها از ۲۲۰ تا ۳۸۸ نوکلئوتید تشکیل میشوند و RNA آنها هیچ پروتئینی کد نمیکند. ویروزوئیدها ساختاری میلهای با شاخههای انتهایی دارند. سر چکشی شکل این پاتوژنها آنزیم ریبوزیمی است و وظیفه جدا کردن رشتههای چندزیرواحدی RNA در همانندسازی را بر عهده دارد. ویروزوئیدها برخلاف ویروئیدها در سیتوپلاسم و با استفاده از RNA پلیمرازهای سلول میزبان تکثیر میشوند. عملکرد ویروزوئیدها شبیه RNAهای ماهوارهای است که سلولهای جانوری را آلوده میکند. ویروس هپاتیت دلتا از انواع RNA ماهوارهای است.
تفاوت ویروئید و پریون
پریونها پاتوژنهای پروتئینی کوچکتر از ویروسها هستند و RNA یا DNA همراه آنها نیست. این گلیکوپروتئینها در حالت طبیعی به لیپیدهای گلیکوزیل فسفاتیدیل اینوزیتول غشای سلول وصل میشوند و به انجام فرایندهای فیزیولوژیک کمک میکنند. تغییر تاخوردگی و کنفورماسیون ساختار سهبعدی، این پروتئین را به پاتوژنی تبدیل میکند که ساختار پروتئینهای دیگر را تغییر میدهد. پریونهای غیربیمازیزا ($$PrP^C$$) در بافتهای مختلف بدن بیان میشوند، اما فراوانی آنها در سیستم عصبی مرکزی و محیطی بیشتر است. این پروتئینها در آکسون رشتههای عصبی سمپاتیک و پاراسمپاتیک به انتقال پیشرونده و پسرونده مواد بین جسم سلولی و پایانه آکسون کمک میکنند.
ساختار پریون چیست؟
انتهای N پریونهای طبیعی ساختار انعطافپذیری است که از ۸ واحد تکراری (آمینواسیدهای ۲۳-۱۲۰) تشکیل شده است. انتهای C (آمینواسیدهای ۱۲۱-۲۳۱) این پروتئینها از ۳ هلیکس آلفا و ۲ صفحه بتا تشکیل میشود. سیستئین ۱۷۹ و ۲۱۴ این پروتئینها با پیوند دیسولفیدی بهم وصل شده است و گروههای گلیکوزیلی به آمینواسیدهای ۱۸۱ و ۱۹۷ متصل میشود. این ساختار در پریونهای بیماریزا $$(PrP^{Sc})$$ به تعداد زیادی صفحه بتا تبدیل میشود. این ($$PrP^{Sc}$$ بهوسیله دومین پروتئازی از غشا جدا شده و توده تشکیل میدهند. عامل بیماریهای کروتزفلد جاکوب یا جنون گاوی، سندرم گرسمن-استراسلر-شانکر، بیخوابی کشنده خانوادگی و بیماری کورکو در انسان پریونها هستند. این بیماریها با از دست دادن حافظه، محدود شدن حرکت، زوال عقل، تغییر شخصیت و اسفنجی شدن بافت مغز همراه است و ممکن است از گوشت حیوانات آلوده به انسان منتقل شود.

تفاوت ویروئید و ویروس چیست؟
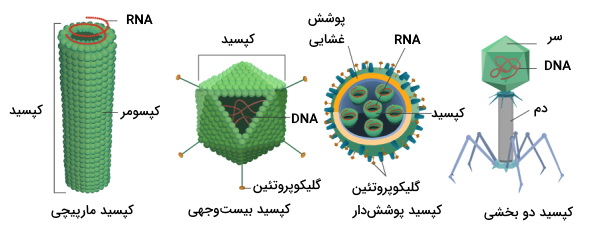
ویروسها پاتوژنهای بسیار کوچکی هستند که از اسید نوکلئیک (RNA یا DNA) و پوشش پروتئینی تشکیل شدهاند. این پاتوژنها برای رشد و تکثیر به آنزیمها، ساختارهای پروتئینی و مسیرهای متابولیکی پروکاریوتها، گیاهان یا جانوران نیاز دارند. در ژنوم ویروسها برخلاف ویروئیدها و ویروزوئیدها کدهای پروتئین وجود دارد. ویروسها بر اساس مورفولوژی کپسید به انواع رشتهای، دو بخشی (سر و گردن)، چندوجهی و پوششدار تقسیم میشوند. این پاتوژنها را میتوان بر اساس نوع ماده ژنتیکی به انواع DNA ویروسها و RNA ویروسها تقسیمبندی کرد.
ماده ژنتیکی ممکن است تکرشتهای یا دورشتهای و حلقوی یا خطی باشد. ژنوم ویروسها از یک مولکول اسیدنوکلئیک، یا چند مولکول کوچک اسید نوکلئیک باشد. پروتئینهای کپسید، پروتئینهای اتصالی به غشا و تعداد کمی از آنزیمها از رونویسی ژنوم ویروسی سنتز میشود. غشای سلولهای پوششدار بخشی از غشای سلول میزبان با تغییراتی جزئی است که دور لایهای از پروتئینهای اتصالی به غشا قرار دارد. در سطح خارجی این غشا، گلیکوپروتئینهایی به نام پلومر وجود دارد که در اتصال ویروس به غشا و تحریک سیستم ایمنی میزبان نقش دارد.
ورود ویروس به سلول
برای ورود به سلول میزبان پروتئینها کپسید یا غشای ویروسها به گیرندههای سلول میزبان متصل میشود. در بعضی از ویروسها ازجمله HIV و HPV اتصال گیرنده-پروتئین با ادغام غشای ویروس و میزبان همراه است. در نتیجه ماده ژنتیکی و کپسید وارد سلول میشود. در بعضی از ویروسها ازجمله هپاتیت C و پولیو پروتئین به گیرندههای اندوسیتوزی متصل شده و ویروس کامل به سیتوپلاسم میزبان منتقل میشود. در بعضی از ویروسها ازجمله باکتریوفاژها اتصال گیرنده-پروتئین با انتقال کپسید همراه ماده ژنتیکی یا ماده ژنتیکی تنها به سیتوپلاسم میزبان همراه است. پس از ورود به سیتوپلاسم پوشش پروتئینی باید از ماده ژنتیکی جدا شود. تغییر pH اندوزوم سبب تغییر کنفورماسیون و دناتوره شدن کپسید ویروسهایی میشود که با اندوسیتوز منتقل شدهاند.
همانندسازی اسید نوکلئیک ویروس
ویروسها بر اساس نوع ماده ژنتیکی بهوسیله مکانیسمهای متفاوت و در بخشهای مختلف سلول همانندسازی میکنند. در بعضی از ویروسها ژنوم RNA ابتدا به DNA تبدیل و سپس بهوسیله آنزیمهای میزبان یا ویروس همانندسازی میشود. ژنوم بعضی از ویروسها پس از ورود به DNA میزبان همانندسازی میشود.
DNA ویروسهای دورشتهای
ماده ژنتیکی این ویروسها شبیه تمام موجودات زنده است. DNA این ویروسها با استفاده از آنزیمهای پلیمراز میزبان در هسته همانندسازی میشود. RNA پلیمراز II میزبان این ژنوم را رونویسی میکند و mRNA با مکانیسمهای پس از رونویسی سلول میزبان اصلاح میشود. پروتئین ژنهایی که در مرحله اول کد میشوند به افزایش کارایی همانندسازی و رونویسی ژنهای تاخیری کمک میکنند. ژنهای تاخیری به تشکیل ویروس کامل و آزادش شدن ویروس از میزبان کمک میکنند و پس از همانندسازی DNA ترجمه میشوند.

DNA ویروسهای تکرشتهای
بیشتر ویروسهای ssDNA (به جز ویروسهای انسانی آنولوویرید و پارووویریدها) باکتریها و سلولهای گیاهی را آلوده میکنند. ssDNA پس از ورود به هسته میزبان در مرحله S چرخه سلولی بهوسیله آنزیمهای پلیمراز به DNA دورشته تبدیل میشود. بخشی از ssDNA این ویروسها ساختار سنجاقسری دارد و پرایمر پلیمرازها است. در مرحله بعد RNA و DNA پلیمراز ژنوم دورشتهای ویروس را رونویسی و همانندسازی میکنند.
RNA ویروسهای دورشتهای
ماده ژنتیکی این ویروسها چند مولکول RNA کوچک است و خارج از هسته همانندسازی میشود. RNA پلیمراز وابسته به RNA همراه ویروس، از رشته منفی ژنوم رونویسی میکند. این آنزیم ویژگی ویرایش RNA را ندارد. به همین دلیل فراوانی جهش در RNA ویروسها از DNA ویروسها بیشتر است. ماده ژنتیکی این ویروسها کامل از کپسید جدا نمیشود و mRNA رونویسی شده از منافذ کپسید به سیتوپلاسم منتقل میشود. همزمان با تشکیل شدن کپسید جدید، RNA پلیمراز وابسته به RNA نسخه مکمل mRNA را میسازد و ویروس جدید تشکیل میشود.
RNA ویروسهای تکرشتهای مثبت
ژنوم این ویروسها mRNA حاوی کدهای پروتئین ویروس است و بدون تغییر بهوسیله سیستم آنزیمی میزبان ترجمه میشود. ژن RNA پلیمراز وابسته به RNA در ژنوم این ویروسها وجود دارد و بلافاصله پس ورود به سلول ترجمه میشود. در بعضی از ویروسهای ssRNA یک پلیپپتید بلند از ترجمه ژنوم تشکیل و بهوسیله پروتئازها به زنجیرههای کوچکتر تجزیه میشود. در همانندسازی ژنوم، ابتدا نسخه منفی RNA سنتز میشود. سپس RNA پلیمراز وابسته به RNA رشته مکمل (ژنوم) را همانندسازی میکند.
RNA ویروسهای تکرشتهای منفی
ژنوم این ویروسها نسخه مکمل mRNA است و RNA پلیمراز وابسته به RNA در کپسید وجود دارد. در مرحله اول RNA پلیمراز وابسته به RNA ژنوم منفی را در سیتوپلاسم به mRNA تبدیل میکند و ژنهای اولیه بهوسیله آنزیمهای میزبان ترجمه میشود. در همانندسازی ژنوم، ابتدا باید نسخه مکمل مثبت سنتز شود. این نسخه با mRNA اولیه تفاوت دارد و فاقد $$5^prime CAP$$ و توالی پلی A است. پرتئینهای ویروسی به جایگاه پایان پلیمراز یا آنزیم پلیمراز متصل شده و رونویسی را مهار میکنند. در این شرایط همانندسازی ژنوم شروع میشود.
RNA ویروسهای رونوشت معکوس
ژنوم رتروویروسها، دو مولکول RNA تکرشتهای مثبت است. برخلاف سایر ویروسها، هر ژن رتروویروسها از دو نسخه مشابه تشکیل شده و دیپلوئید است. همراه این ژنوم آنزیم رونوشتبردار معکوس (RT) در کپسید وجود دارد. پس از ورود به سیتوپلاسم سلول، رونوشتبردار معکوس با رونویسی ژنوم، DNA دو رشتهای مکمل سنتز میکند. این DNA وارد ژنوم میزبان شده و همانندسازی میشود. در دو انتهای RNA این ویروسها توالیهای تکراری ویژهای وجود دارد. این توالیها در ورود cDNA به ژنوم میزبان نقش دارند. آنزیم رونوشتبردار معکوس رتروویروسها از دو رشته پلیپپتیدی با اندازههای متفاوت تشکیل شده است و فعالیت DNA پلیمراز وابسته به RNA، DNA پلیمراز وابسته به DNA و RNAase H دارد. اما مثل پلیمراز سایر ویروسها توانایی ویرایش RNA یا DNA را ندارد.
در کپسید این ویروسها تعداد زیادی از tRNA میزبان قبلی وجود دارد که پرایمر RT است. برای شروع رونویسی tRNA باز شده و با پیوند هیدروژنی به ۱۸ نوکلئوتید انتهای $$5^prime$$ متصل میشود. RT به پرایمر متصل شده و DNA مکمل ژنوم (رشته منفی) را رونویسی میکند. در مرحله بعد RT تمام RNA ویروسی به جز توالی پورینی انتهای $$5^prime$$ را تجزیه میکند. RT از این توالی به عنوان پرایمر استفاده کرده و رشته مکمل DNA منفی را در جهت $$5^primerightarrow3^prime$$ همانندسازی میکند. اینتگراز یکی دیگر از آنزیمهای همراه رترویروسها است که در DNA میزبان و ویروسی برش ایجاد میکند. برش ایجاد شده پس از ورود DNA ویروسی به میزبان بهوسیله آنزیمهای میزبان ترمیم میشود. DNA ویروسی همراه میزبان بهوسیله آنزیم RNA پلیمراز II رونویسی میشود و بخشی از آن در کپسیدهای تازه سنتز شده قرار میگیرد.
DNA ویروسهای رونوشت معکوس
ژنوم ویروسهای «کالیموویرید» (Caulimoviridae) گیاهان و «هپادناویرید» (Hepadnaviridae) جانوران DNA حلقوی است. بخشی از این DNA دورشتهای و بخش دیگر آن تکرشتهای است. رشته ناقص ژنوم مثبت است. این رشته پس از ورود به هسته میزبان کامل و حلقه بسته میشود. ژنوم این ویروسها وارد ژنوم میزبان نمیشود. mRNA ویروسی بهوسیله RNA پلیمراز II میزبان از رشته منفی DNA رونویسی و از هسته خارج میشود. در DNA حلقوی دو جایگاه تکراری (DR1 و DR2) یکسان وجود دارد.
RNA پلیمراز رونویسی را از منطقه بالادست اولین جایگاه تکراری شروع و پس از یک دور کامل در پایین دست این جایگاه تمام میکند. در نتیجه دو طرف mRNA حاصل توالی تکراری وجود دارد که بخشی از این توالی یک لوپ تشکیل میدهد. آنزیم رونوشتبردار معکوس به این بخش متصل شده و چند نوکلئوتید اول را به عنوان پرایمر رونویسی میکند. رونویسی RNA تا انتها ادامه دارد و در نهایت رشته DNA منفی مکمل mRNA سنتز میشود. آنزیم رونوشتبردار معکوس تمام RNA به جز بخش کوچکی که حاوی توالی DR1 است را تجزیه میکند. این توالی به انتهای دیگر DNA منتقل و به DR2 متصل میشود. رونوشتبردار معکوس از این توالی به عنوان پرایمر استفاده و رشته مثبت DNA را همانندسازی میکند.
خروج ویروس از میزبان
ویروسهای پوششدار نزدیک غشای پلاسمایی، شبکه اندوپلاسمی یا دستگاه گلژی سرهمبندی میشود. برهمکنش پروتئینهای کپسید این ویروسها با غشا سبب خم شدن غشا و جوانه زدن ویروس میشود. اما ویروسهای بدون پوشش در بخشهای مختلف سیتوپلاسم سرهمبندی و بهوسیله اگزوسیتوز از میزبان خارج میشوند. ویروسهای لیتیک غشای پلاسمایی راپاره میکنند و همزمان با لیز شدن سلول، از میزبان خارج میشوند.
سوالات متداول
در این بخش از مطلب مجله فرادرس به تعدادی از سوالات متداول پیرامون ویروئید پاسخ میدهیم.
ویروئید کوتولگی رازک چیست؟
«ویروئید کوتولگی رازک» (Hop Stunt Viroid) یکی از اعضای خانواده پوسپی ویروئیدها است که گیاه رازک، درخت مرکبات و درخت انگور را آلوده میکند. آلودگی این ویروئید منجر به کندی رشد گیاهان و رشد برگها به طرف پایین میشود. این ویروئید ممکن است از راه ابزارهای کشاورزی و کارگران به سایر گیاهان منتقل شود. ضدعفونی کردن وسایل، ابزارها و دست و حذف گیاهان آلوده، از انتقال ویروئید به گیاهان سالم پیشگیری میکند.
درمان پریون چیست؟
بیماریهای ایجاد شده بهوسیله پریونها با انجام MRI، تست مایع مغزی-نخاعی، الکتروآنسفالوگرافی، آزمایش خون و نمونهبرداری از بافت عصبی تشخیص داده میشود. این پروتئینها به گرما، مواد شیمیایی و اشعه مقاوم هستند و درمان مشخصی برای آنها وجود ندارد.
source